
通讯作者:宋继彬,北京化工大学;付钦瑞,青岛大学
作者:付钦瑞,隗闯,杨潇,王梦真,宋继彬
正文内容:
目前的放射治疗缺乏准确区分肿瘤组织和健康组织的能力,导致患者遭受严重的放射损伤。因此,迫切需要精准的放疗技术,以优化肿瘤控制,同时最大限度地减少对周围健康组织的不良影响。在这项研究中,作者开发了一种由弗林酶响应的RVRR肽偶联的金纳米棒组成的纳米药物(AuNR@Peptide),它将可激活的成像探针和放射增敏剂整合到一个系统中,用于精确的肿瘤定位,实现图像指导的精准放疗。静脉给药后,生物标志物(弗林酶)对AuNR@Peptide上的RVRR底物进行蛋白水解,触发金纳米棒组装成更大的聚集体,由于金纳米粒子间的等离子耦合效应从而激活近红外二区光声信号,此外,粒径更大的聚集体通过阻止金纳米棒的迁移和回流来增强其瘤内滞留,从而提高其辐射敏感性。注射后在肿瘤部位观察到近红外二区光声信号的峰值时间点可作为启动X-射线辐射时间点的参考,并通过与放射增敏机制相关的研究阐明增敏机制,体内实验表明其放疗效果有实质性改善。本研究将影像与治疗相结合,为肿瘤提供了一种有前景的影像指导治疗方式。
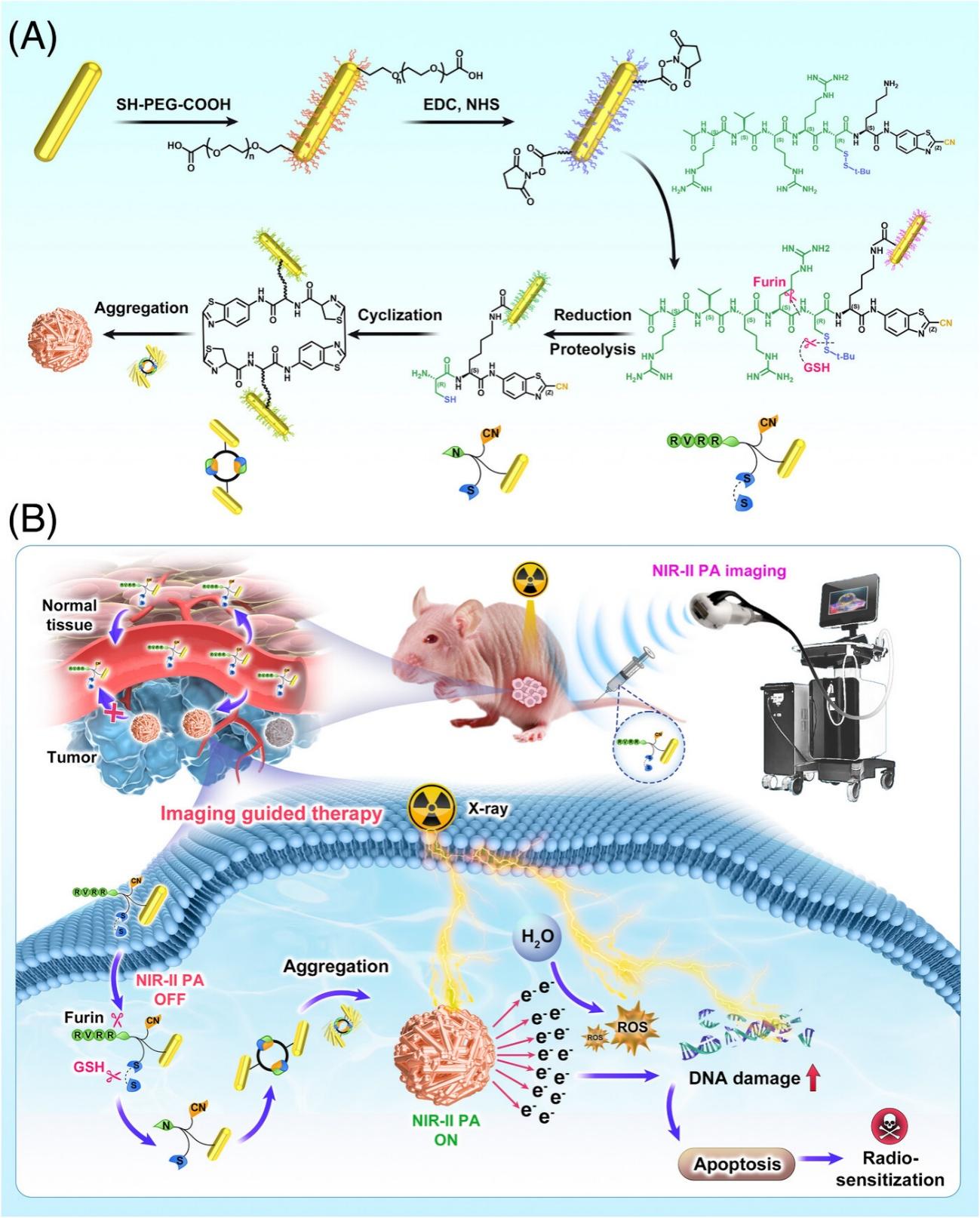
图1. (A) AuNR@Peptide纳米药物的制造流程示意图,(B)生物标志物响应的近红外二区光声成像指导的放射增敏的工作机制。
以上研究性论文以“Biomarker-induced gold aggregates enable activatable near-infrared-II photoacoustic image-guided radiosensitization”为题发表于Aggregate期刊(中科院一区,IF=13.9),论文通讯作者为北京化工大学宋继彬教授和青岛大学付钦瑞教授。